潰瘍性大腸炎に対する生物学的製剤
旧ブログの方に記載していた内容をこちらにも掲載します。
言葉の定義
生物学的製剤
生物学的製剤とは、バイオテクノロジー(遺伝子組換え技術や細胞培養技術)を用いて製造された薬剤で、特定の分子を標的とした治療のために使われるものです。
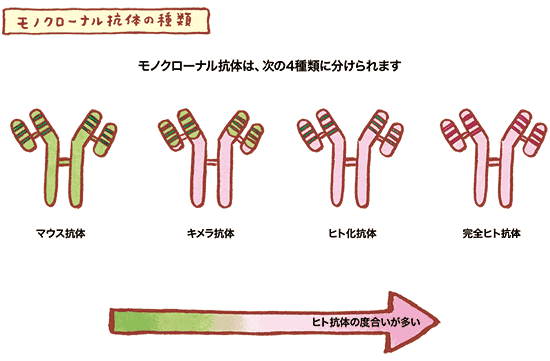
モノクローナル抗体
体内に侵入した細菌やウイルスなどの異物(抗原)から体を守るために「抗体」がつくられます。 抗原にあるたくさんの目印(抗原決定基)の中から1種類(モノ)の目印とだけ結合する抗体を、 人工的にクローン(クローナル)増殖させたものをモノクローナル抗体といいます。分子標的薬など、がん細胞の特定の抗原に結合する薬などに利用されています
キメラ
生物学における キメラ (chimera) とは、同一の個体内に異なる遺伝情報を持つ細胞が混じっている状態のことです。
キメラは、ギリシア神話に登場する頭がライオンで胴体が山羊である生物「キマイラ」に由来しています。
インフリキシマブは上の図で、頭部がマウスによるもので胴体がヒト由来であるためキメラ抗体と言われます。頭部が炎症起因物質である TNF-α に結合します。
マブ(mab) とは?
mab とは monoclonal antibodyの略です。
以下のような命名規則があるようです。
さらにその前に、対象疾患や臓器を示すサブステムがつけられます。腫瘍(tumor)に対する医薬であれば「-ta-」(2017年以前は「-tu-」)、 免疫系に作用するものなら「-li-」がつくという具合です。ここに、開発者が自由につけられる接頭辞が加えられて、医薬としての一般名となります。
インフリキシマブの名はinf-li-xi-mabと分解でき、免疫系に作用するキメラ抗体であることがわかります。
アダリムマブは ada-li-mu-mab と分解できますが、上の説明だと ada-li-u-mab になりそうなところですが、どういうわけかこういう命名になっています。
それぞれの最初の部分は、薬剤ごとの個別識別要素で特別な意味はないようです。
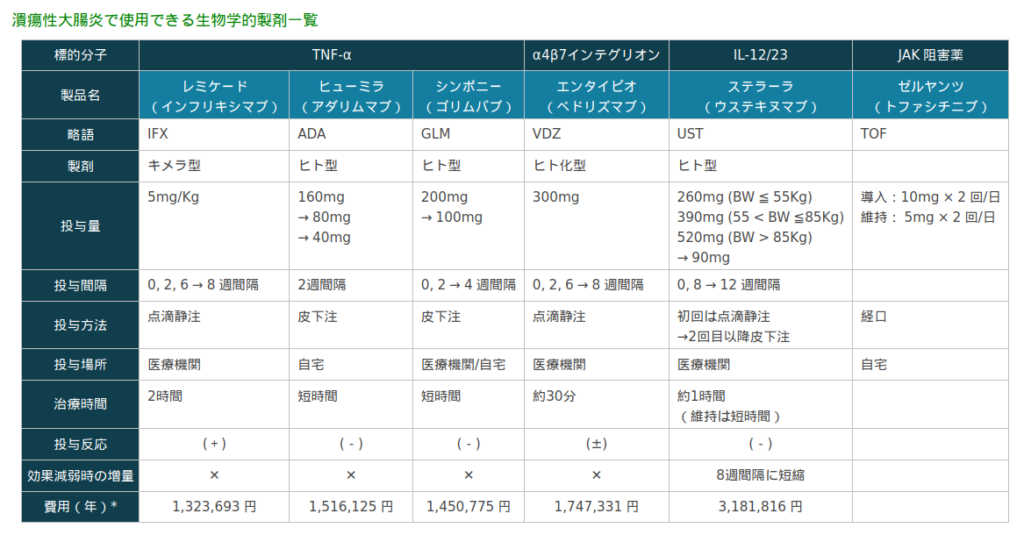
潰瘍性大腸炎の生物学的製剤
3 年ほど前に作成したものでちょっと古いですが。
この他に、ミリキズマブとグセルクマブが現在使用できるようです。
インフリキシマブ(レミケード)
投与8週後における有効率は約7割・寛解率は約3割と生物学的製剤の中では最も有効率が高い。 難治性の潰瘍性大腸炎でも比較的重症のタイプ、速やかに寛解導入したい場合に使用されることが多い。
キメラ抗体なのでアレルギーが出現することがある。
長期投与による有効率の低下は抗体出現によるものと考えられ、アザチオプリンを併用することで効果維持が期待できる。
アダリムマブ(ヒュミラ)
アダリムマブはヒト型抗体であるため、キメラ型抗体であるインフリキシマブにおいて注意すべき投与時反応がほとんどない抗TNF – α 製剤である。
投与方法は皮下注で自己注射できるため自宅で投与することができ、インフリキシマブのように 2 – 3 時間かけて病院内で点滴静注する必要はない。
インフリキシマブとは異なりアザチオプリンの併用による有効率の改善は認められないため、 比較的中等症やアザチオプリンが使用しにくい患者・自宅で自己注射を希望する場合に適応となる。
ゴリムバブ(シンポニー)
アダリムマブと同様にヒト型抗体であり、自己注射も可能である。 比較的中等症でステロイド抵抗例などの難治性の潰瘍性大腸炎に適応がある。
インフリキシマブやアダリムマブを使用した後で、2 nd・3 rd で使用されることが多い。
ベドリズマブ(エンタイビオ)
上の 3 剤は抗TNF – α 製剤であるが、ベドリズマブは α4β7 インテグリンに対する抗体である。
抗TNF – α 製剤は潰瘍性大腸炎の治療薬として有効な薬剤ではあるが、一定の割合で無効例が存在するため、 それらに対する新しい機序を有する薬剤として開発されたのがベドリズマブである。 腸管選択的な抗炎症作用を持つ。
重症感染症や悪性腫瘍の関連が低く安全性が高いとされており、高齢者や免疫抑制療法を既に実施されている症例への使用が望ましい。
投与方法は点滴静注であるが実施時間は 30 分と短い。
ウステキヌマブ(ステラーラ)
上に提示した薬剤とは作用点が異なり、IL-12/23 の p40 に対するヒト化モノクローナル抗体である。
寛解維持療法における有効性・安全性が高いとされており、また維持療法における投与間隔が 12 週と長いため、病勢が比較的緩やかで仕事や学業で忙しい症例が良い適応となる。
トファシチニブ(ゼルヤンツ)
米国ファイザー社によって開発された世界初のヤヌスキナーゼ(Janus kinase : JAK)阻害薬で経口投与が可能な分子標的薬である。
免疫源性も低く効果減弱が起きにくい薬剤とされ、有効率も抗TNF – α 製剤とほぼ同等とされている。
投与対象は、「過去の治療において、他の薬物療法(ステロイド、免疫抑制剤又は生物製剤)による適切な治療を行っても、 疾患に起因する明らかな臨床症状が残る場合に投与すること。」となっている。
半減期は非常に短く、また血中濃度測定の必要はない。ただし、帯状疱疹などの合併症が多いと言われている。 また、免疫調節薬との併用は禁忌で妊婦にも使用できない。
これらの薬剤の使い分け
比較的重症で速やかに寛解導入したい場合はインフリキシマブ、中等症で寛解導入を急ぐ場合でなければ各製剤を患者の要求などに応じて使用すれば良いと思われる。
抗TNF – α 製剤の一次無効例では、抗TNF – α 製剤 → 抗TNF – α 製剤への変更による効果はあまり期待できず、ベドリズマブ・ウステキヌマブ・トファシチニブなどに変更する。
無効例とトラフ濃度
生物学的製剤が無効な例はある程度存在し、最初から効果が不十分な一次無効例と最初は十分な効果があったもののその後は効果が不十分となる二次無効例があります。
二次無効例は、おそらく生物学的製剤に対する抗体が産生されることによるトラフ濃度の低下が関与していると考えられています。
トラフ濃度とは、定常状態最低血中濃度のことで、薬剤投与によって血中濃度は急速に上昇し、その後時間の経過とともに薬剤濃度は低下するので、 通常は次回投与直前の濃度を示しています。
つまり、抗体産生によって血中濃度の低下が速くなり、効果が減弱するのです。
この二次無効例はどの薬剤にも起こり、その割合に大きな差はないと言われています。
生物学的製剤はやめることができるのか?
潰瘍性大腸炎での生物学的製剤中止後の経過に関する報告はネット検索では見つかりませんでしたが、RAとクローンに関する情報はありました。
RAでは深い寛解に達した後であれば中止後の寛解維持率は約80%とのこと。
クローン病では寛解後に中止すると寛解が維持できるのは20%、しかも再発後にレミケードを再開してもレミケード治療に対して抵抗性が出現してくるようで、 少なくともクローン病に関する限り生物学的製剤は中止しない方がいいと思われます。